2实验结果与分析
2.1不同Mg2+浓度对pH的影响
不同的Mg2+浓度下,阴极室pH在上述4组实验中随时间的变化分别如图2中(a)、(b)、(c)及(d)所示。
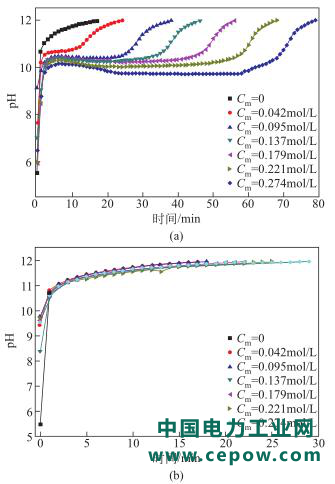
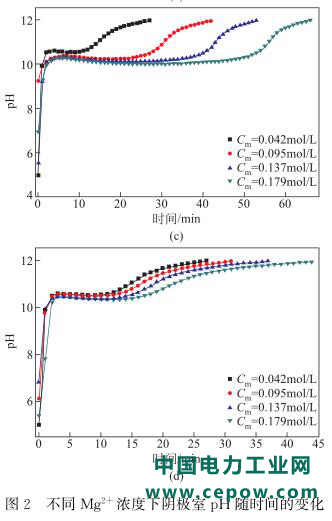
由图2可知,随着电解过程的进行,阴极液的pH在电解初期上升很快,图2(a)、(c)和(d)中存在平稳期,且图2(a)和图2(c)中该平稳期的时长随着Mg2+浓度的增大而增加,而图2(b)中并没有产生平稳期,图2(d)中的平稳期时长基本相同。平稳期的产生主要由于Mg2+与OH-会结合形成沉淀析出,消耗了OH-,从而导致pH不升高。
图2(b)中没有产生平稳期是因为虽然阴极室溶液中不含Mg2+,但中间室溶液中的Mg2+会穿过阳离子膜到达阴极室,与OH-结合形成沉淀,此时并没有将OH-消耗完全,但是会使pH的升高减缓;图2(d)中平稳期的时长基本相同,这是由于此时阴极室溶液中Mg2+浓度相同。当pH再次升高时,此时溶液中的Mg2+已基本消耗完,所以随着电解的进行,阴极液的pH又逐渐升高。
图2(a)中可以看出当阴极液全部为MgCl2溶液(Cm=0.274mol/L)时,阴极液的pH基本保持在9.8左右,此时即为Mg2+随着电解的进行不断形成沉淀析出的过程。当Mg2+消耗完全阴极液的pH又逐渐升高,随着Mg2+浓度的增加,pH达到11.96时的电解时长也随之增加。